Sie haben in die beste Matratze investiert. Ihr Schlafzimmer ist eine schallisolierte Festung der Dunkelheit, optimiert auf exakt 18 Grad. Sie schlucken Magnesium, meiden blaues Licht und tracken jede REM-Phase mit hochpräzisen Wearables. Und doch: Wenn Sie nachts wach liegen und das Gedankenkarussell an Fahrt aufnimmt, fühlen Sie sich Ihrem eigenen Nervensystem hilflos ausgeliefert.
Das Problem ist ein „Broken System“. Wir optimieren die äußeren Rahmenbedingungen, ignorieren aber den fundamentalsten biologischen Prozess unseres Körpers: die Atmung. Rund 20.000 Mal am Tag atmen wir ein und aus – meist völlig unbewusst. Doch genau hier liegt die Schnittstelle zwischen Körper und Geist, die einzige Funktion des autonomen Nervensystems, die wir willentlich steuern können.
In diesem Artikel erfahren Sie, warum die herkömmliche Empfehlung, „einfach mal tief durchzuatmen“, physiologisch oft kontraproduktiv ist, und wie Sie durch gezielte, wissenschaftlich fundierte Atemtechniken Ihre Schlafarchitektur von Grund auf neu programmieren.
Der am häufigsten missverstandene Rat lautet: „Atmen Sie tief ein.“ Physiologisch gesehen ist dies bei akutem Stress oft kontraproduktiv. Eine forcierte Einatmung triggert die Dehnungsrezeptoren der Lunge, die (wenn falsch ausgeführt) den Sympathikus – Ihren Fluchtmodus – eher stimulieren als beruhigen (Busch et al., 2012).
Zudem riskieren Sie eine Hypokapnie (CO2-Untersättigung). Ohne ausreichend Kohlendioxid im Blut bleibt der Sauerstoff an Ihr Hämoglobin gebunden, anstatt in Ihre Zellen und Ihr Gehirn zu diffundieren. Sie atmen viel, aber Ihr Gehirn „erstickt“ energetisch. Die Folge ist das klassische nächtliche Herzrasen und ein hyperaktiver Geist (Ringer et al., 2019, 2020; Lum, 1981; 2022; Duffin et al., 2019; Tolin et al., 2022; Papp et al., 1993; Cardim et al., 2024).
Die drei Dimensionen des Atems: Mehr als nur Gasaustausch
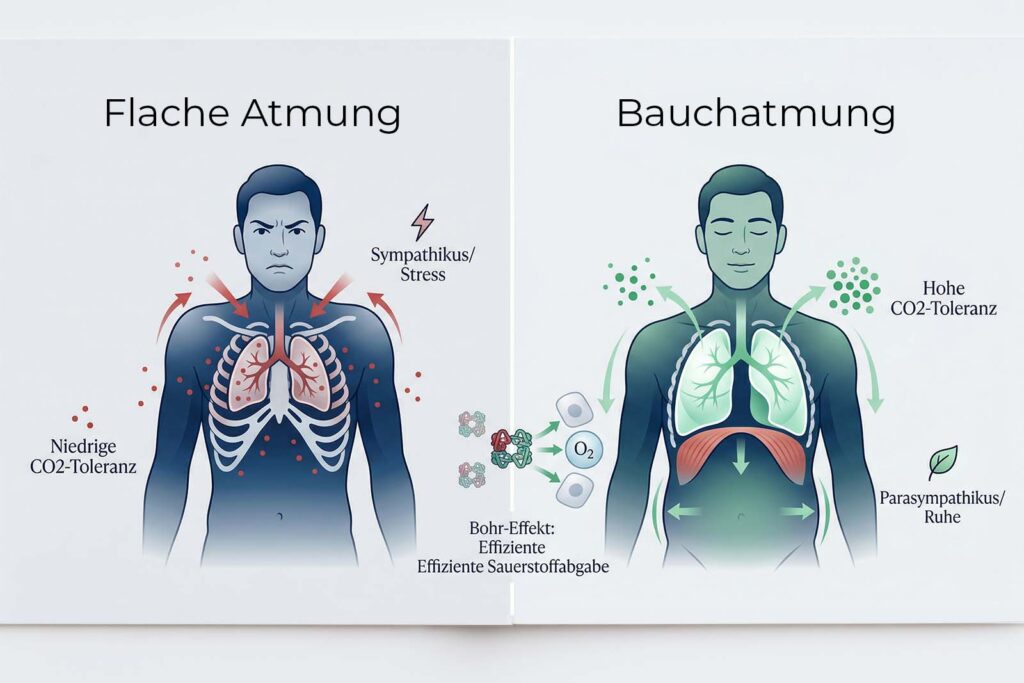
Um zu verstehen, warum Atemtraining tiefer geht als jede Entspannungs-App, müssen wir die Atmung in drei wissenschaftliche Säulen unterteilen:
Die drei Säulen der respiratorischen Reintegration
Um Ihre Schlafarchitektur nachhaltig zu verändern, müssen wir drei Ebenen synchronisieren, die ich in meiner Arbeit als die „Respiratorische Triade“ bezeichne:
1. Die biochemische Dimension (CO2-Toleranz als Resilienz-Marker)
Ihr Atemantrieb wird nicht durch Sauerstoffmangel gesteuert, sondern durch Ihre Sensibilität gegenüber Kohlendioxid. Wer chronisch gestresst ist, hat eine niedrige CO2-Toleranz. Schon ein geringer Anstieg nachts führt zu gesteigerten Mikrowachreaktionen oder unruhigen Träumen (Georgopoulos et al., 2024; Vaporidi et al., 2019; Guyenet & Bayliss, 2015; Grandmont et al., 2025; Lüthi & Nedergaard, 2025; Antila et al., 2022; Kalmbach et al., 2018; Soffer-Dudek, 2017).
Es herrscht ein weitverbreiteter Irrtum: Sauerstoff sei „gut“ und Kohlendioxid (CO2) lediglich ein „Abfallprodukt“. Die Physiologie lehrt uns das Gegenteil. Der Bohr-Effekt besagt, dass Sauerstoff nur dann effizient von den roten Blutkörperchen an das Gewebe und das Gehirn abgegeben werden kann, wenn eine ausreichende Konzentration an CO2 im Blut vorhanden ist (Valsecchi et al., 2026; Dash et al., 2015; Sekyonda et al., 2024).
Wer unter Dauerstress steht, atmet oft zu viel (chronische Hyperventilation). Dies führt zu einem CO2-Mangel (Hypokapnie), wodurch der Sauerstoff paradoxerweise fester am Hämoglobin bindet und die Zellen – inklusive der Gehirnzellen – schlechter versorgt werden. Die Folge: Innere Unruhe und Erschöpfung trotz Schlaf (Suess et al., 1980; Masaoka & Homma, 1997; Cluff, 1984; Ristiniemi et al., 2014; Ramakers et al., 2022).
Die Lösung: Wir müssen Ihr Chemorezeptoren-System „umprogrammieren“. Techniken wie die 4-7-8-Methode sind hier keine Entspannungsübungen, sondern ein gezieltes Training, um die Amygdala chemisch zu desensibilisieren.
2. Die biomechanische Dimension (Das Zwerchfell als Vagus-Pumpe)
Die meisten Menschen nutzen nur das obere Drittel ihrer Lungenkapazität. Diese flache Brustatmung ist ein mechanisches Signal für „Gefahr“ (Jerath & Beveridge, 2020; Hernando et al., 2016; Pervichko et al., 2022; Zaliene et al., 2025; Faull et al., 2019; Hood, 2023; Guyenet, 2014).
Ihr Zwerchfell ist nicht nur ein Atemmuskel, sondern ein mechanischer Kolben. Bei korrekter Funktion massiert es die inneren Organe, unterstützt den venösen Rückstrom des Blutes zum Herzen und pumpt Lymphflüssigkeit (Bordoni et al., 2016; Salah et al., 2022; Fogarty & Sieck, 2019; Sieck & Fogarty, 2025; Abu-Hijleh et al., 1995; Kocjan et al., 2018). Viele Menschen sind jedoch „Brustatmer“. Sie nutzen ihre Atemhilfsmuskulatur im Nacken und in den Schultern, was dem Gehirn permanent eine Fluchtsituation signalisiert und Nackenschmerzen verursacht.
Das Zwerchfell steht in direkter anatomischer Verbindung zum Vagusnerv. Eine korrekte Zwerchfellbewegung wirkt wie ein mechanischer Stimulus auf diesen Ruhe-Nerv. In meinem Protokoll lernen Sie, das Zwerchfell als „Kolben“ zu nutzen, der den Cortisolspiegel physisch nach unten reguliert.
3. Die psychophysiologische Dimension (Bottom-Up statt Top-Down)
Affirmationen und „positives Denken“ versagen oft, wenn der Körper im Überlebensmodus ist. Die Neurobiologie zeigt: Der Atem ist die Fernbedienung für Ihren Vagusnerv. Etwa 80 % der Fasern des Vagusnervs sind afferent – das bedeutet, sie senden Signale vom Körper zum Gehirn. Der Großteil, weit mehr als 50% aller Informationen fließen vom Körper zum Gehirn (Afferenz) (Iba et al., 2025; Berthoud et al., 2025; Cameron, 2009; Gershon & Margolis, 2021; Schulz & Vögele, 2015; Quadt et al., 2018; Critchley & Garfinkel, 2017; Feldman et al., 2024; Critchley & Garfinkel, 2018; Münzberg et al., 2023; Quigley et al., 2021).
Wenn Sie Ihren Atem verändern, senden Sie ein „Bottom-up“-Signal direkt in das Stammhirn: „Gefahr vorbei, Schlafmodus an.“
Die Strategie: Durch Techniken wie den Physiologischen Seufzer oder Resonanzatmung (5,5 Atemzüge/Min.) nutzen wir die „Bottom-Up“-Kommunikation. Wir überzeugen das Gehirn über die Biologie, dass es sicher ist, die Kontrolle abzugeben.
Die „Schlaf-Matrix“: Techniken im Labor-Check
Warum die 4-7-8-Methode kein Trick, sondern Pharmakologie ist
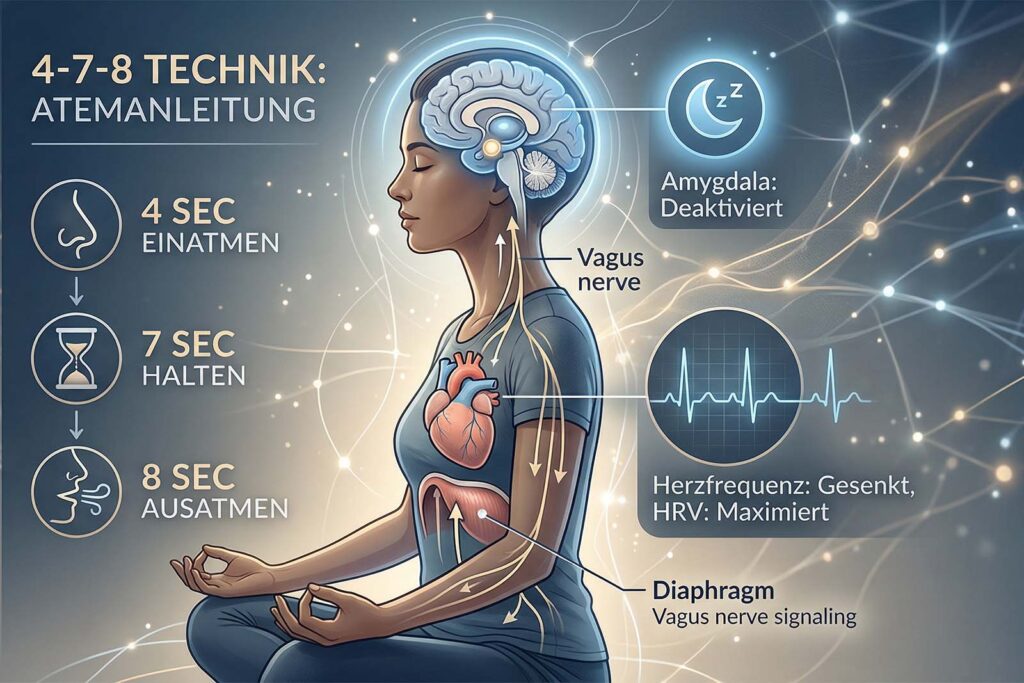
Die populäre 4-7-8-Technik wird oft als „Einschlaf-Trick“ belächelt. Neurobiologisch betrachtet ist sie jedoch eine präzise pharmakologische Intervention. 4-7-8: Pharmakologie ohne Nebenwirkungen
Diese Technik nutzt die Verlängerung der Ausatemphase, um den Baroreflex zu aktivieren. Es ist eine gezielte Manipulation Ihres Blutdrucks und Ihrer Herzrate. Wir nutzen hier die Sinusarrhythmie: Beim Ausatmen verlangsamt das Herz natürlich. Durch das 8-sekündige Ausatmen dehnen wir diese Ruhephase künstlich aus, bis das Gehirn keine andere Wahl hat, als in den parasympathischen Modus zu schalten.
Der Mechanismus: Durch das lange Anhalten des Atems (7 Sekunden) und das noch längere Ausatmen (8 Sekunden) erhöhen Sie kontrolliert den CO2-Gehalt in Ihrem Blut. Dies senkt die Aktivität der Amygdala, dem Angstzentrum Ihres Gehirns.
Die Wirkung: Es erhöht die CO2-Toleranz Ihres Nervensystems. Ein hoher CO2-Spiegel signalisiert dem Parasympathikus (dem „Ruhenerv“), die Herzfrequenz massiv zu senken. Es wirkt wie ein biologisches Beruhigungsmittel, das die neurochemische Kaskade von Stresshormonen unterbricht (Zaccaro et al., 2018; Bentley et al., 2023; Noble & Hochman, 2019; Jerath et al., 2019; Laborde et al., 2019; Sévoz-Couche & Laborde, 2022; Shao et al., 2024; Sakurai et al., 2023; Balban et al., 2023).
Transient Hypofrontality: Den „inneren Kritiker“ schlafen legen
Eines der größten Hindernisse beim Einschlafen ist der präfrontale Kortex – der Sitz unseres logischen Denkens, Planens und Grübelns. Atemtechniken, die auf einen rhythmischen, leicht forcierten Fokus setzen, können einen Zustand der „Transient Hypofrontality“ induzieren.
Indem wir die Aufmerksamkeit massiv auf den Atemrhythmus lenken, wird die Aktivität im präfrontalen Kortex kurzzeitig reduziert. Der „innere Kritiker“ wird leiser, das Gedankenkarussell kommt zum Stillstand. Dies ist die biologische Voraussetzung für das Loslassen und den Übergang in die Delta-Wellen des Tiefschlafs (Tomasino & Fabbro, 2016; Doll et al., 2016; Dickenson et al., 2012; Angioletti & Balconi, 2024; Zheng et al., 2019; Balconi & Angioletti, 2022.
Der „Physiologische Seufzer“: Stanfords schnellste Methode gegen akuten Stress
Dr. Andrew Huberman von der Stanford University hat den Cyclic Sighing (physiologischen Seufzer) als einen schnellen und sehr effektiven Weg identifiziert, um das Nervensystem in Echtzeit herunterzufahren (Balban et al., 2023; Vaschillo et al., 2015; Onyper et al., 2025; Hanley et al., 2025; Hanley et al., 2025; Vlemincx et al., 2013).
Die Technik: Zweimal kurz hintereinander durch die Nase einatmen (der zweite Atemzug füllt die kollabierten Lungenbläschen, die Alveolen, wieder auf) und dann lange und langsam durch den Mund ausatmen.
Warum es funktioniert: Diese Methode maximiert die Oberfläche für den Gasaustausch und stößt das angesammelte CO2 effizient aus, was den Herzschlag sofort verlangsamt. Es ist der biologische Reset-Knopf für Momente akuter Panik vor dem Einschlafen.
Die Biochemie des Summens: Stickstoffmonoxid und Melatonin
Eine Technik aus der Yoga-Tradition (Bhramari), die heute wissenschaftlich validiert ist, ist das Summen beim Ausatmen.
Das Summen beim Ausatmen erhöht die Stickstoffmonoxid-Konzentration in den Nasennebenhöhlen um den Faktor 15 (Weitzberg & Lundberg, 2002; Sikka, 2023; Eby, 2006; Lundberg, 2008). NO ist ein potenter Vasodilatator. Es entspannt die glatte Muskulatur und bereitet den Körper auf die Thermregulation vor – das notwendige Absinken der Kerntemperatur für den Tiefschlaf.
NO wirkt gefäßerweiternd, antimikrobiell und beruhigend Maniscalco et al., 2003; Sikka, 2023; Lundberg, 2008). Die erhöhte NO-Konzentration verbessert die Sauerstoffaufnahme in der Lunge (Fan et al., 2018; Hardeland et al., 2011; Blanco et al., 2025; Bredt, 1999) und scheint indirekt die Melatonin-Produktion zu unterstützen, indem sie den Körper in einen tiefen Entspannungszustand versetzt.
Temperaturregulation durch den Atem
Um einschlafen zu können, muss die Körperkerntemperatur sinken. Die Körperkerntemperatur sinkt beim Einschlafen messbar. Wichtig sind die Richtung und die Geschwindigkeit des Abfalls. Schon sehr kleine, gezielte Änderungen der Hauttemperatur können die Einschlaflatenz um ~25 % verkürzen (Raymann et al., 2005; Haghayegh et al., 2022).
Im Sommer oder bei innerer Hitze (z.B. durch Stress) fällt dies schwer. Hier helfen die Kühltechniken Sheetali oder Sitkari.
Durch das Einatmen über die gerollte Zunge oder durch die Zähne wird die Luft befeuchtet und abgekühlt, bevor sie die Lungen erreicht. Dieser thermische Reiz wirkt über den Vagusnerv direkt auf das Thermoregulationszentrum im Hypothalamus und signalisiert dem Körper: „Zeit für die Nachtruhe“.
Schlafapnoe & Nasenatmung: Funktionelles Training der Atemwege
Viele Menschen leiden unter leichten Formen der Schlafapnoe oder Schnarchen, oft bedingt durch eine schwache Oropharynx-Muskulatur und chronische Mundatmung (Koka et al., 2021; De Felicio et al., 2018; Lv et al., 2023; Yang et al., 2025; Hoang et al., 2023; Silva et al., 2024; Schramm et al., 2024).
Die Umstellung auf strikte Nasenatmung (ggf. unterstützt durch „Mouth Taping“ in der Nacht) und gezieltes Training der Zungenposition (Mewing) kann die oberen Atemwege stabilisieren. Die Nase filtert, wärmt und befeuchtet nicht nur die Luft, sondern reguliert auch den Atemwiderstand, was die Tiefschlafphasen stabilisiert.
Psychosomatik: Emotionales Detox im Delta-Zustand
Schlafstörungen können mit „unterdrückten“ bzw. dysregulierten Emotionen zusammenhängen, sind aber nicht einfach nur deren Resultat. Typisch ist eine Wechselwirkung: schwierige Emotionen und ungünstige Strategien (z.B. Unterdrückung, Grübeln) verschlechtern den Schlaf – und schlechter Schlaf schwächt wiederum die Fähigkeit, Emotionen gesund zu verarbeiten. Intensivere Formen der Atemarbeit, wie das holotrope Atmen, können eventuell diese Traumata an die Oberfläche bringen.
Strategie für Resilienz: Die 3-6-5 Methode
Um dauerhaft besser zu schlafen, reicht eine Übung direkt vor dem Bettgehen oft nicht aus. Das Nervensystem muss über den Tag konditioniert werden. Die 3-6-5 Methode ist hier der Goldstandard:
3 Mal am Tag
6 Atemzüge pro Minute (Resonanzfrequenz)
5 Minuten lang
Diese rhythmische Konditionierung nivelliert den Cortisolspiegel über den Tag hinweg, sodass Sie abends nicht mit einem „überreizten“ System ins Bett gehen. Es ist die ultimative Burnout-Prävention durch biologische Rhythmisierung.
Self-Check: Wie effizient atmen Sie wirklich?
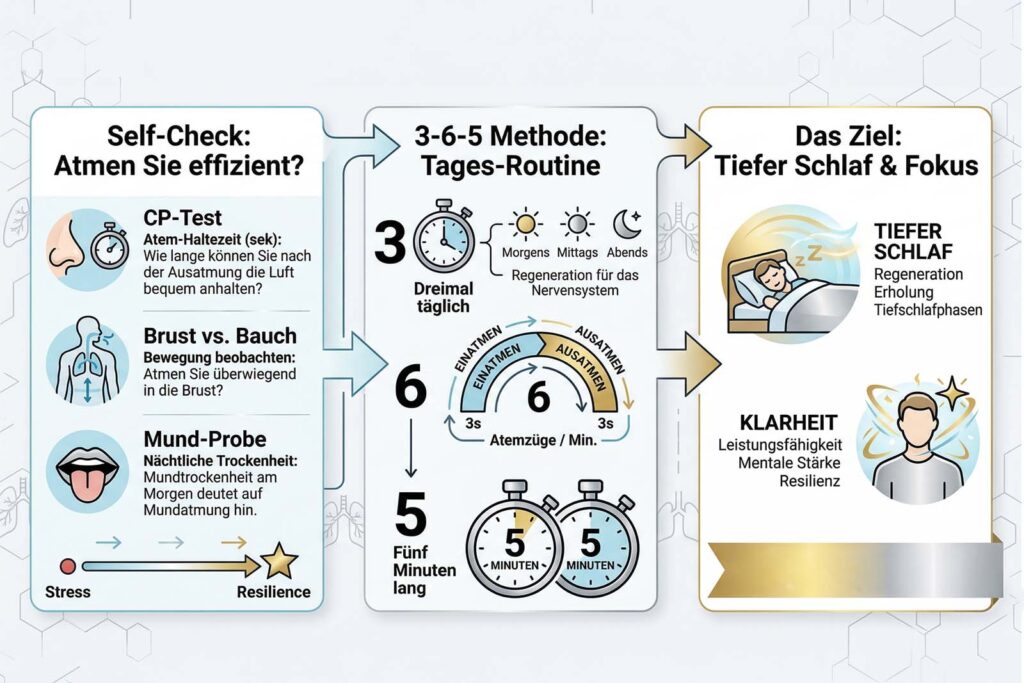
Nehmen Sie sich kurz Zeit für diesen wissenschaftlichen Selbsttest:
Der CP-Test (Control Pause): Atmen Sie normal aus und halten Sie die Luft an (ohne zu forcieren). Wie viele Sekunden vergehen, bis der erste deutliche Einatmen-Impuls kommt?
Unter 20 Sek.: Ihr System ist auf Stress programmiert, Ihre CO2-Toleranz ist niedrig.
Über 40 Sek.: Ihr Stoffwechsel ist effizient und stressresistent.
Brust vs. Bauch: Legen Sie eine Hand auf die Brust, eine auf den Bauch. Welche Hand bewegt sich zuerst? Wenn es die obere ist, befinden Sie sich im biomechanischen Überlebensmodus.
Die Mund-Probe: Wachen Sie morgens mit trockenem Mund auf? Wenn ja, verlieren Sie nachts wertvolle Energie durch Mundatmung und dehydrieren Ihr Gehirn.
Wenn Sie professionelle Unterstützung möchten, geht´s hier zum Atemaudit.
Fazit: Ihr Atem als Investition
Schlafstörungen sind keine Schwäche, sondern ein Signal Ihres biologischen Systems, das die Verbindung zur eigenen Regulation verloren hat. Atemtraining ist kein Wellness, sondern angewandte Neurowissenschaft.
Indem Sie die drei Dimensionen des Atems – Biochemie, Biomechanik und Psychophysiologie – meistern, übernehmen Sie die Kontrolle über Ihre nächtliche Regeneration. Es ist die nachhaltigste Investition in Ihre Gesundheit, Ihre kognitive Leistungsfähigkeit und Ihre Lebensqualität.
Hören Sie auf, den Schlaf zu erzwingen. Schaffen Sie stattdessen die biologischen Voraussetzungen, unter denen Ihr Körper gar nicht anders kann, als in tiefen, erholsamen Schlaf zu sinken.
Warum Wissen allein keine Lösung ist
Sie können die Chemie des Schlafes verstehen, aber Ihr Nervensystem ist wie ein Muskel: Es braucht keine Information, sondern Konditionierung.
Die meisten Menschen scheitern, weil sie Techniken nur dann anwenden, wenn sie bereits wach liegen. Das ist so, als würde man versuchen, während eines Sturms das Segeln zu lernen. Wahre respiratorische Souveränität entsteht durch rhythmische Konditionierung.
Wir müssen das Nervensystem über einen Zeitraum von mehreren Wochen „umschulen“, damit die korrekte, schlaffördernde Atmung zu Ihrer neuen Standard-Einstellung (Default Mode) wird. Erst wenn die biochemische Toleranz erhöht und die biomechanische Effizienz wiederhergestellt ist, wird Schlaf von einer Anstrengung zu einem natürlichen Resultat.
Das Circadian Breath System: Ihr Nervensystem im Rhythmus
Schlafqualität wird nicht erst im Bett entschieden, sondern durch die Summe Ihrer Atemzüge über den Tag hinweg. Das Circadian Breath System ist ein wissenschaftlich fundiertes Audio-Training, das Ihr Nervensystem rhythmisch konditioniert. Diese fünf „Bio-Pacer“ nehmen Sie an die Hand: Ohne Sekunden zu zählen, folgen Sie einfach den akustischen Signalen, um Ihre Biochemie und Ihr Stresslevel gezielt zu steuern.
Nutzen Sie die untenstehenden Hörproben, um ein Gefühl für die Frequenzen und die Führung zu bekommen.
Modul 1: Morning Power – Der metabolische Wecker
Fokus: Stoffwechsel-Aktivierung & CO2-Toleranz.
Starten Sie Ihren Tag nicht mit künstlichem Stress, sondern mit biologischer Energie. Durch 30 kraftvolle Atemzyklen und gezielte Atemphasen fluten wir Ihre Zellen mit Sauerstoff und programmieren Ihr System auf Wachheit und Resilienz. Die ideale Basis für einen Tag ohne Energietiefs.
- Technik: Dynamische Bauchatmung & Retention.
- Dauer: ca. 6 Minuten.
Hören Sie hier kurz rein:
Modul 2: Deep Focus – Deine Insel der Klarheit
Fokus: Kognitive Präzision & Mentale Ruhe.
Wenn die Aufgaben überhandnehmen, sorgt Deep Focus für den nötigen „Reset“ im Gehirn. Die quadratische Taktung (Box Breathing) stabilisiert Ihre Herzrate und beruhigt das emotionale Zentrum Ihres Gehirns. Ideal vor wichtigen Meetings oder um aus dem Multitasking-Chaos auszusteigen.
- Technik: Box Breathing (4-4-4-4).
- Dauer: 5 Minuten.
Hören Sie hier kurz rein:
Modul 3: HRV-Sync – Die Welle der Harmonie
Fokus: Herzratenvariabilität & Innere Balance.
Bringen Sie Herz und Lunge in perfekte Resonanz. Dieses Modul nutzt die Frequenz von 5,5 Sekunden, um Ihren Vagusnerv sanft zu stimulieren. Es wirkt wie eine innere Massage für Ihr Nervensystem und baut das Stresshormon Cortisol bereits über den Mittag effektiv ab.
- Technik: Kohärente Resonanzatmung.
- Dauer: 5 Minuten.
Hören Sie hier kurz rein:
Modul 4: Work-Life-Reset – Die Tür zum Feierabend
Fokus: Stress-Entladung & Emotionaler Übergang.
Schließen Sie die Tür zum Arbeitstag auch mental. Mithilfe des „Physiologischen Seufzers“ – der schnellsten Methode der Wissenschaft, um Stress in Echtzeit abzubauen – befreien wir Ihr System von angestautem Druck. Damit der Feierabend dort beginnt, wo er hingehört: in Ihrer Entspannung.
- Technik: Cyclic Sighing (Doppel-Einatmung).
- Dauer: 5 Minuten.
Hören Sie hier kurz rein:
Modul 5: Nightfall – Deine Brücke in den Schlaf
Fokus: Melatonin-Boost & Tiefschlaf-Vorbereitung.
Das finale Modul bereitet Ihren Körper chemisch auf das Loslassen vor. Die Kombination aus der 4-7-8-Technik und sanftem Summen (Humming) weitet Ihre Gefäße und signalisiert Ihrem Gehirn absolute Sicherheit. Die Gedanken kommen zur Ruhe, der Körper wird schwer – bereit für eine Nacht voller Regeneration.
- Technik: 4-7-8 Methode & Bhramari (Summen).
- Dauer: 20 Minuten (ideal zum Einschlafen).
Hören Sie hier kurz rein:
🎧 Zeit für den nächsten Schritt?
Sie haben einen ersten Einblick erhalten. Dieser Inhalt ist Teil unseres exklusiven All-Access-Bereichs, in dem wir tief in die Biologie und Psychologie Ihrer mentalen Performance eintauchen.
Als Abonnent erhalten Sie sofort:
- Unbegrenzten Zugriff auf alle Audio-Trainings & Experten-Artikel.
- Exklusive Inhalte zu den Themen Atmung, Fokus und Burnout-Prävention usw.
- Automatischen Zugang zu allen zukünftigen Erweiterungen.
Bereits Mitglied? [Hier einloggen]
Abdelfatah, D., Ahmed, D., Amer, M., Harby, S., & Abdelaty, H. (2024). The Effect of Deep Breathing Exercise versus 4-7-8 Breathing Technique on Insomnia, Pain, and Anxiety Among Patients with Burn Injuries. Egyptian Journal of Nursing and Health Sciences. https://doi.org/10.21608/ejnhs.2024.382869
Abu-Hijleh, M., Habbal, O., & Moqattash, S. (1995). The role of the diaphragm in lymphatic absorption from the peritoneal cavity.. Journal of anatomy, 186 ( Pt 3), 453-67.
Adhikari, N., Burns, K., Friedrich, J., Granton, J., Cook, D., & Meade, M. (2007). Effect of nitric oxide on oxygenation and mortality in acute lung injury: systematic review and meta-analysis. BMJ : British Medical Journal, 334, 779. https://doi.org/10.1136/bmj.39139.716794.55
Aktaş, G., & İlgin, V. (2022). The Effect of Deep Breathing Exercise and 4–7-8 Breathing Techniques Applied to Patients After Bariatric Surgery on Anxiety and Quality of Life. Obesity Surgery, 33, 920-929. https://doi.org/10.1007/s11695-022-06405-1
Angioletti, L., & Balconi, M. (2024). Boosting Prefrontal Brain Responsiveness by Interoceptive Attentiveness during Synchronized Breathing, Motor, and Cognitive Task. Psychiatry International. https://doi.org/10.3390/psychiatryint5020017
Arora, D., & Bhatla, S. (2017). Melatonin and nitric oxide regulate sunflower seedling growth under salt stress accompanying differential expression of Cu/Zn SOD and Mn SOD. Free Radical Biology and Medicine, 106, 315–328. https://doi.org/10.1016/j.freeradbiomed.2017.02.042
Bach, V., Delanaud, S., Barcat, L., Bodin, E., Tourneux, P., & Libert, J. (2019). Distal skin vasodilation in sleep preparedness, and its impact on thermal status in preterm neonates.. Sleep medicine. https://doi.org/10.1016/j.sleep.2018.12.026
Balban, M., Neri, E., Kogon, M., Weed, L., Nouriani, B., Jo, B., Holl, G., Zeitzer, J., Spiegel, D., & Huberman, A. (2023). Brief structured respiration practices enhance mood and reduce physiological arousal. Cell Reports Medicine, 4. https://doi.org/10.1016/j.xcrm.2022.100895
Balban, M., Neri, E., Kogon, M., Weed, L., Nouriani, B., Jo, B., Holl, G., Zeitzer, J., Spiegel, D., & Huberman, A. (2023). Brief structured respiration practices enhance mood and reduce physiological arousal. Cell Reports Medicine, 4. https://doi.org/10.1016/j.xcrm.2022.100895
Balconi, M., & Angioletti, L. (2022). Interoceptive Attentiveness Induces Significantly More PFC Activation during a Synchronized Linguistic Task Compared to a Motor Task as Revealed by Functional Near-Infrared Spectroscopy. Brain Sciences, 12. https://doi.org/10.3390/brainsci12030301
Benke, C., Hamm, A., & Pané-Farré, C. (2017). When dyspnea gets worse: Suffocation fear and the dynamics of defensive respiratory responses to increasing interoceptive threat.. Psychophysiology, 54 9, 1266-1283. https://doi.org/10.1111/psyp.12881
Bentley, T., D’Andrea-Penna, G., Rakic, M., Arce, N., LaFaille, M., Berman, R., Cooley, K., & Sprimont, P. (2023). Breathing Practices for Stress and Anxiety Reduction: Conceptual Framework of Implementation Guidelines Based on a Systematic Review of the Published Literature. Brain Sciences, 13. https://doi.org/10.3390/brainsci13121612
Berthoud, H., Münzberg, H., Morrison, C., & Neuhuber, W. (2025). Gut-brain communication: Functional anatomy of vagal afferents. Current Opinion in Neurobiology, 93. https://doi.org/10.1016/j.conb.2025.103058
Bigatello, L., Hurford, W., Kacmarek, R., Roberts, J., & Zapol, W. (1994). Prolonged Inhalation of Low Concentrations of Nitric Oxide in Patients with Severe Adult Respiratory Distress Syndrome: Effects on Pulmonary Hemodynamics and Oxygenation. Anesthesiology, 80, 761-770. https://doi.org/10.1097/00000542-199404000-00007
Birdee, G., Nelson, K., Wallston, K., Nian, H., Diedrich, A., Paranjape, S., Abraham, R., & Gamboa, A. (2023). Slow breathing for reducing stress: The effect of extending exhale. Complementary therapies in medicine, 73, 102937 – 102937. https://doi.org/10.1016/j.ctim.2023.102937
Blanco, S., Del Mar Muñoz-Gallardo, M., Hernández, R., & Peinado, M. (2025). The Interplay Between Melatonin and Nitric Oxide: Mechanisms and Implications in Stroke Pathophysiology. Antioxidants, 14. https://doi.org/10.3390/antiox14060724
Bordoni, B., Marelli, F., Morabito, B., & Sacconi, B. (2016). Manual evaluation of the diaphragm muscle. International Journal of Chronic Obstructive Pulmonary Disease, 11, 1949 – 1956. https://doi.org/10.2147/copd.s111634
Bredt, D. (1999). Endogenous nitric oxide synthesis: biological functions and pathophysiology.. Free radical research, 31 6, 577-96. https://doi.org/10.1080/10715769900301161
Busch, V., Magerl, W., Kern, U., Haas, J., Hajak, G., & Eichhammer, P. (2012). The effect of deep and slow breathing on pain perception, autonomic activity, and mood processing–an experimental study.. Pain medicine, 13 2, 215-28. https://doi.org/10.1111/j.1526-4637.2011.01243.x
Cameron, O. (2009). Visceral brain–body information transfer. NeuroImage, 47, 787-794. https://doi.org/10.1016/j.neuroimage.2009.05.010
Cardim, D., Giardina, A., Ciliberti, P., Battaglini, D., Berardino, A., Uccelli, A., Czosnyka, M., Roccatagliata, L., Matta, B., Patroniti, N., Rocco, P., & Robba, C. (2024). Short-term mild hyperventilation on intracranial pressure, cerebral autoregulation, and oxygenation in acute brain injury patients: a prospective observational study. Journal of Clinical Monitoring and Computing, 38, 753 – 762. https://doi.org/10.1007/s10877-023-01121-2
Cespuglio, R., Amrouni, D., Meiller, A., Buguet, A., & Gautier-Sauvigné, S. (2012). Nitric oxide in the regulation of the sleep-wake states.. Sleep medicine reviews, 16 3, 265-79. https://doi.org/10.1016/j.smrv.2012.01.006
Cluff, R. (1984). Chronic Hyperventilation and its Treatment by Physiotherapy: Discussion Paper. Journal of the Royal Society of Medicine, 77, 855 – 862. https://doi.org/10.1177/014107688407701011
Critchley, H., & Garfinkel, S. (2017). Interoception and emotion.. Current opinion in psychology, 17, 7-14. https://doi.org/10.1016/j.copsyc.2017.04.020
Critchley, H., & Garfinkel, S. (2018). The influence of physiological signals on cognition. Current Opinion in Behavioral Sciences, 19, 13-18. https://doi.org/10.1016/j.cobeha.2017.08.014
Dash, R., & Bassingthwaighte, J. (2004). Blood HbO2 and HbCO2 Dissociation Curves at Varied O2, CO2, pH, 2,3-DPG and Temperature Levels. Annals of Biomedical Engineering, 32, 1676-1693. https://doi.org/10.1007/s10439-004-7821-6
Dash, R., Korman, B., & Bassingthwaighte, J. (2015). Simple accurate mathematical models of blood HbO2 and HbCO2 dissociation curves at varied physiological conditions: evaluation and comparison with other models. European Journal of Applied Physiology, 116, 97 – 113. https://doi.org/10.1007/s00421-015-3228-3
De Felicio, C., Da Silva Dias, F., Folha, G., De Almeida, L., De Souza, J., Anselmo-Lima, W., Trawitzki, L., & Valera, F. (2016). Orofacial motor functions in pediatric obstructive sleep apnea and implications for myofunctional therapy.. International journal of pediatric otorhinolaryngology, 90, 5-11. https://doi.org/10.1016/j.ijporl.2016.08.019
De Felicio, C., Dias, F., & Trawitzki, L. (2018). Obstructive sleep apnea: focus on myofunctional therapy. Nature and Science of Sleep, 10, 271 – 286. https://doi.org/10.2147/nss.s141132
Dempsey, J., & Gibbons, T. (2023). Rethinking O2, CO2 and breathing during wakefulness and sleep. The Journal of Physiology, 602. https://doi.org/10.1113/jp284551
Dempsey, J., Smith, C., Przybylowski, T., Chenuel, B., Xie, A., Nakayama, H., & Skatrud, J. (2004). The ventilatory responsiveness to CO2 below eupnoea as a determinant of ventilatory stability in sleep. The Journal of Physiology, 560. https://doi.org/10.1113/jphysiol.2004.072371
Dickenson, J., Berkman, E., Arch, J., & Lieberman, M. (2012). Neural correlates of focused attention during a brief mindfulness induction.. Social cognitive and affective neuroscience, 8 1, 40-7. https://doi.org/10.1093/scan/nss030
Doll, A., Hölzel, B., Bratec, S., Boucard, C., Xie, X., Wohlschläger, A., & Sorg, C. (2016). Mindful attention to breath regulates emotions via increased amygdala–prefrontal cortex connectivity. NeuroImage, 134, 305-313. https://doi.org/10.1016/j.neuroimage.2016.03.041
Duffin, J., Hare, G., & Fisher, J. (2019). A mathematical model of cerebral blood flow control in anaemia and hypoxia. The Journal of Physiology, 598. https://doi.org/10.1113/jp279237
Eby, G. (2006). Strong humming for one hour daily to terminate chronic rhinosinusitis in four days: a case report and hypothesis for action by stimulation of endogenous nasal nitric oxide production.. Medical hypotheses, 66 4, 851-4. https://doi.org/10.1016/j.mehy.2005.11.035
Fabbro, D., Bornhardt-Suazo, T., Schönbeck, A., De Meyer, M., & Lavigne, G. (2024). Understanding the clinical management of co‐occurring sleep‐related bruxism and obstructive sleep apnea in adults: A narrative and critical review. Journal of Prosthodontics, 34, 46 – 61. https://doi.org/10.1111/jopr.13966
Fan, W., He, Y., Guan, X., Gu, W., Wu, Z., Zhu, X., Huang, F., & He, H. (2018). Involvement of the nitric oxide in melatonin‐mediated protection against injury. Life Sciences, 200, 142–147. https://doi.org/10.1016/j.lfs.2018.03.035
Farb, N., Zuo, Z., & Price, C. (2023). Interoceptive Awareness of the Breath Preserves Attention and Language Networks amidst Widespread Cortical Deactivation: A Within-Participant Neuroimaging Study. eNeuro, 10. https://doi.org/10.1523/eneuro.0088-23.2023
Faull, O., Jenkinson, M., Ezra, M., & Pattinson, K. (2016). Conditioned respiratory threat in the subdivisions of the human periaqueductal gray. eLife, 5. https://doi.org/10.7554/elife.12047
Faull, O., Subramanian, H., Ezra, M., & Pattinson, K. (2019). The midbrain periaqueductal gray as an integrative and interoceptive neural structure for breathing. Neuroscience & Biobehavioral Reviews, 98, 135-144. https://doi.org/10.1016/j.neubiorev.2018.12.020
Feldman, M., Bliss-Moreau, E., & Lindquist, K. (2024). The neurobiology of interoception and affect. Trends in Cognitive Sciences, 28, 643-661. https://doi.org/10.1016/j.tics.2024.01.009
Finck, N., Pacheco, M., & De Araújo, M. (2024). Association of clinical indicators in TMJ, craniofacial, occlusal, and upper airway changes with symptoms of pediatric obstructive sleep apnea and mouth-breathing. CRANIO®, 43, 802 – 808. https://doi.org/10.1080/08869634.2024.2356631
Fogarty, M., & Sieck, G. (2019). Evolution and Functional Differentiation of the Diaphragm Muscle of Mammals.. Comprehensive Physiology, 9 2, 715-766. https://doi.org/10.1002/cphy.c180012
Francis, G., Petrovic, P., Lundström, J., & Thunell, E. (2024). Induction of nitric oxide via humming does not improve short-term cognitive performance or influence emotional processing. PLOS ONE, 19. https://doi.org/10.1371/journal.pone.0301268
Franzini, D., Cuny, L., & Pierce-Talsma, S. (2018). Osteopathic Lymphatic Pump Techniques. Journal of Osteopathic Medicine Journal of Osteopathic Medicine, 118, e43 – e44. https://doi.org/10.7556/jaoa.2018.112
Ganesan, S., Moffat, B., Van Dam, N., Lorenzetti, V., & Zalesky, A. (2023). Meditation attenuates default-mode activity: A pilot study using ultra-high field 7 Tesla MRI. Brain Research Bulletin, 203. https://doi.org/10.1016/j.brainresbull.2023.110766
Georgopoulos, D., Bolaki, M., Stamatopoulou, V., & Akoumianaki, E. (2024). Respiratory drive: a journey from health to disease. Journal of Intensive Care, 12. https://doi.org/10.1186/s40560-024-00731-5
Gerlach, H., Rossaint, R., Pappert, D., & Falke, K. (1993). Time‐course and dose‐response of nitric oxide inhalation for systemic oxygenation and pulmonary hypertension in patients with adult respiratory distress syndrome. European Journal of Clinical Investigation, 23. https://doi.org/10.1111/j.1365-2362.1993.tb00797.x
Gershon, M., & Margolis, K. (2021). The gut, its microbiome, and the brain: connections and communications.. The Journal of clinical investigation, 131 18. https://doi.org/10.1172/jci143768
Grandmont, C., Karamaoun, C., Martin, S., & Noël, F. (2025). Sensitivity and optimality analysis of breathing scenarios for 1D or 0D models of gas diffusion in the lung.. Journal of theoretical biology, 615, 112235. https://doi.org/10.1016/j.jtbi.2025.112235
Granqvist, S., Sundberg, J., Lundberg, J., & Weitzberg, E. (2006). Paranasal sinus ventilation by humming.. The Journal of the Acoustical Society of America, 119 5 Pt 1, 2611-7. https://doi.org/10.1121/1.2188887
Grundy, D. (2002). Neuroanatomy of visceral nociception: vagal and splanchnic afferent. Gut, 51, i2 – i5. https://doi.org/10.1136/gut.51.suppl_1.i2
Guimaraes, K., Drager, L., Genta, P., Marcondes, B., & Lorenzi-Filho, G. (2009). Effects of oropharyngeal exercises on patients with moderate obstructive sleep apnea syndrome.. American journal of respiratory and critical care medicine, 179 10, 962-6. https://doi.org/10.1164/rccm.200806-981oc
Guyenet, P. (2014). Regulation of breathing and autonomic outflows by chemoreceptors.. Comprehensive Physiology, 4 4, 1511-62. https://doi.org/10.1002/cphy.c140004
Guyenet, P., & Bayliss, D. (2015). Neural Control of Breathing and CO2 Homeostasis. Neuron, 87, 946-961. https://doi.org/10.1016/j.neuron.2015.08.001
Haghayegh, S., Khoshnevis, S., Smolensky, M., Hermida, R., Castriotta, R., Schernhammer, E., & Diller, K. (2022). Novel temperature‐controlled sleep system to improve sleep: a proof‐of‐concept study. Journal of Sleep Research, 31. https://doi.org/10.1111/jsr.13662
Haghayegh, S., Smolensky, M., Khoshnevis, S., Hermida, R., Castriotta, R., & Diller, K. (2021). The Circadian Rhythm of Thermoregulation Modulates both the Sleep/Wake Cycle and 24 h Pattern of Arterial Blood Pressure.. Comprehensive Physiology, 11 4, 1-14. https://doi.org/10.1002/cphy.c210008
Hanley, A., Davis, A., Worts, P., & Pratscher, S. (2025). Cyclic sighing in the clinic waiting room may decrease pain: results from a pilot randomized controlled trial. Journal of Behavioral Medicine, 48, 385 – 393. https://doi.org/10.1007/s10865-024-00548-5
Hardeland, R., Cardinali, D., Srinivasan, V., Spence, D., Brown, G., & Pandi‑Perumal, S. (2011). Melatonin—A pleiotropic, orchestrating regulator molecule. Progress in Neurobiology, 93, 350-384. https://doi.org/10.1016/j.pneurobio.2010.12.004
Harding, E., Franks, N., & Wisden, W. (2019). The Temperature Dependence of Sleep. Frontiers in Neuroscience, 13. https://doi.org/10.3389/fnins.2019.00336
He, H., & He, L. (2020). Crosstalk between melatonin and nitric oxide in plant development and stress responses.. Physiologia plantarum. https://doi.org/10.1111/ppl.13143
Herberger, S., Penzel, T., Fietze, I., Glos, M., Cicolin, A., Fattori, E., Grimaldi, D., Reid, K., Zee, P., Mason, M., & Kräuchi, K. (2024). Enhanced conductive body heat loss during sleep increases slow-wave sleep and calms the heart. Scientific Reports, 14. https://doi.org/10.1038/s41598-024-53839-x
Hernando, A., Lázaro, J., Gil, E., Valdés, A., Rey, J., López-Antón, R., Cámara, C., Laguna, P., Aguiló, J., & Bailón, R. (2016). Inclusion of Respiratory Frequency Information in Heart Rate Variability Analysis for Stress Assessment. IEEE Journal of Biomedical and Health Informatics, 20, 1016-1025. https://doi.org/10.1109/jbhi.2016.2553578
Hoang, D., Le, V., Nguyen, T., & Jagomägi, T. (2023). Orofacial dysfunction screening examinations in children with sleep-disordered breathing symptoms.. The Journal of clinical pediatric dentistry, 47 4, 25-34. https://doi.org/10.22514/jocpd.2023.032
Hood, M. (2023). Respiratory, Autonomic and Emotional Responses to Affect Manipulation in High and Low Trait Anxiety. **.
Hsu, B., Emperumal, C., Grbach, V., Padilla, M., & Enciso, R. (2020). Effects of respiratory muscle therapy on obstructive sleep apnea: A systematic review and meta-analysis. Journal of Clinical Sleep Medicine, 16, 785 – 801. https://doi.org/10.5664/jcsm.8318
Huang, Z., Huang, D., Liu, F., Liang, J., Zhao, Z., Lu, H., Xu, Y., Qiu, Y., & Li, S. (2023). Modified oropharyngeal muscle training and scientific vocalization are effective in treating mild-to-moderate obstructive sleep apnea hypoventilation syndrome in adults. Acta Oto-Laryngologica, 143, 989 – 995. https://doi.org/10.1080/00016489.2023.2288283
Hussain, A., Faheem, B., Jang, H., Lee, D., Mun, B., Rolly, N., & Yun, B. (2024). Melatonin–Nitric Oxide Crosstalk in Plants and the Prospects of NOMela as a Nitric Oxide Donor. International Journal of Molecular Sciences, 25. https://doi.org/10.3390/ijms25158535
Iba, K., Kitano, R., & Iwasaki, Y. (2025). Gut sensing of food ingredients and interoception‐mediated regulation of feeding and glucose metabolism. Physiological Reports, 13. https://doi.org/10.14814/phy2.70636
Jänig, W. (1996). Neurobiology of visceral afferent neurons: neuroanatomy, functions, organ regulations and sensations. Biological Psychology, 42, 29-51. https://doi.org/10.1016/0301-0511(95)05145-7
Jerath, R., & Beveridge, C. (2020). Respiratory Rhythm, Autonomic Modulation, and the Spectrum of Emotions: The Future of Emotion Recognition and Modulation. Frontiers in Psychology, 11. https://doi.org/10.3389/fpsyg.2020.01980
Jerath, R., Beveridge, C., & Barnes, V. (2019). Self-Regulation of Breathing as an Adjunctive Treatment of Insomnia. Frontiers in Psychiatry, 9. https://doi.org/10.3389/fpsyt.2018.00780
Kalmbach, D., Anderson, J., & Drake, C. (2018). The impact of stress on sleep: Pathogenic sleep reactivity as a vulnerability to insomnia and circadian disorders. Journal of Sleep Research, 27. https://doi.org/10.1111/jsr.12710
Kalmbach, D., Cuamatzi-Castelan, A., Tonnu, C., Tran, K., Anderson, J., Roth, T., & Drake, C. (2018). Hyperarousal and sleep reactivity in insomnia: current insights. Nature and Science of Sleep, 10, 193 – 201. https://doi.org/10.2147/nss.s138823
Kocjan, J., Gzik‐Zroska, B., Nowakowska, K., Burkacki, M., Suchoń, S., Michnik, R., Czyżewski, D., & Adamek, M. (2018). Impact of diaphragm function parameters on balance maintenance. PLoS ONE, 13. https://doi.org/10.1371/journal.pone.0208697
Koka, V., De Vito, A., Roisman, G., Petitjean, M., Pignatelli, G., Padovani, D., & Randerath, W. (2021). Orofacial Myofunctional Therapy in Obstructive Sleep Apnea Syndrome: A Pathophysiological Perspective. Medicina, 57. https://doi.org/10.3390/medicina57040323
Kräuchi, K. (2007). The human sleep–wake cycle reconsidered from a thermoregulatory point of view. Physiology & Behavior, 90, 236-245. https://doi.org/10.1016/j.physbeh.2006.09.005
Kräuchi, K. (2007). The thermophysiological cascade leading to sleep initiation in relation to phase of entrainment.. Sleep medicine reviews, 11 6, 439-51. https://doi.org/10.1016/j.smrv.2007.07.001
Kräuchi, K., & Wirz-Justice, A. (2001). Circadian Clues to Sleep Onset Mechanisms. Neuropsychopharmacology, 25, S92-S96. https://doi.org/10.1016/s0893-133x(01)00315-3
Kravchenko, I., Podoksenov, Y., Tyo, M., Kalashnikova, T., Churilina, E., Kozulin, M., Gusakova, A., Kozlov, B., & Kamenshchikov, N. (2024). Prevention of respiratory complications in patients at risk of adverse respiratory events by perioperative nitric oxide delivery during cardiac surgery under cardiopulmonary bypass: a single-center prospective randomized study. Patologiya krovoobrashcheniya i kardiokhirurgiya. https://doi.org/10.21688/1681-3472-2024-3-78-93
Laborde, S., Hosang, T., Mosley, E., & Dosseville, F. (2019). Influence of a 30-Day Slow-Paced Breathing Intervention Compared to Social Media Use on Subjective Sleep Quality and Cardiac Vagal Activity. Journal of Clinical Medicine, 8. https://doi.org/10.3390/jcm8020193
Lang, P., Wangelin, B., Bradley, M., Versace, F., Davenport, P., & Costa, V. (2011). Threat of suffocation and defensive reflex activation.. Psychophysiology, 48 3, 393-6. https://doi.org/10.1111/j.1469-8986.2010.01076.x
Lavalle, S., Masiello, E., Iannella, G., Magliulo, G., Pace, A., Lechien, J., Calvo-Henríquez, C., Cocuzza, S., Parisi, F., Favier, V., Bahgat, A., Cammaroto, G., La Via, L., Gagliano, C., Caranti, A., Vicini, C., & Maniaci, A. (2024). Unraveling the Complexities of Oxidative Stress and Inflammation Biomarkers in Obstructive Sleep Apnea Syndrome: A Comprehensive Review. Life, 14. https://doi.org/10.3390/life14040425
Lee, K., Kim, H., Cho, S., & Joh, J. (2022). Change of Venous Return after Diaphragmatic Deep Breathing. Annals of Phlebology. https://doi.org/10.37923/phle.2022.20.2.95
Lin, H., Su, P., Lin, C., & Hung, C. (2019). Models of anatomically based oropharyngeal rehabilitation with a multilevel approach for patients with obstructive sleep apnea: a meta-synthesis and meta-analysis. Sleep and Breathing, 24, 1279 – 1291. https://doi.org/10.1007/s11325-019-01971-8
Livak, P., & Butkevych, L. (2023). Suction (drainage) principle in classical therapeutic massage.. Shidnoevropejskij zurnal vnutrisnoi ta simejnoi medicini. https://doi.org/10.15407/internalmed2023.02.099
Lum, L. (1981). Hyperventilation and Anxiety State 1. Journal of the Royal Society of Medicine, 74, 1 – 4. https://doi.org/10.1177/014107688107400101
Lundberg, J. (2008). Nitric Oxide and the Paranasal Sinuses. The Anatomical Record: Advances in Integrative Anatomy and Evolutionary Biology, 291. https://doi.org/10.1002/ar.20782
Lüthi, A., & Nedergaard, M. (2025). Anything but small: Microarousals stand at the crossroad between noradrenaline signaling and key sleep functions. Neuron, 113, 509-523. https://doi.org/10.1016/j.neuron.2024.12.009
Lv, R., Liu, X., Zhang, Y., Dong, N., Wang, X., He, Y., Yue, H., & Yin, Q. (2023). Pathophysiological mechanisms and therapeutic approaches in obstructive sleep apnea syndrome. Signal Transduction and Targeted Therapy, 8. https://doi.org/10.1038/s41392-023-01496-3
Magnon, V., Dutheil, F., & Vallet, G. (2021). Benefits from one session of deep and slow breathing on vagal tone and anxiety in young and older adults. Scientific Reports, 11. https://doi.org/10.1038/s41598-021-98736-9
Maniscalco, M. (2006). HUMMING, NITRIC OXIDE AND PARANASAL SINUS VENTILATION. **.
Maniscalco, M. (2017). Nasal nitric oxide as biomarker in the evaluation and management of chronic rhino-sinusitis with nasal polyposis. European Archives of Oto-Rhino-Laryngology, 274, 3817-3818. https://doi.org/10.1007/s00405-017-4591-y
Maniscalco, M., Sofia, M., Weitzberg, E., Carratú, L., & Lundberg, J. (2003). Nasal nitric oxide measurements before and after repeated humming maneuvers. European Journal of Clinical Investigation, 33. https://doi.org/10.1111/j.1365-2362.2003.01277.x
Maniscalco, M., Sofia, M., Weitzberg, E., Laurentiis, G., Stanziola, A., Rossillo, V., & Lundberg, J. (2004). Humming‐induced release of nasal nitric oxide for assessment of sinus obstruction in allergic rhinitis: pilot study. European Journal of Clinical Investigation, 34. https://doi.org/10.1111/j.1365-2362.2004.01384.x
Maniscalco, M., Weitzberg, E., Sundberg, J., Sofia, M., & Lundberg, J. (2003). Assessment of nasal and sinus nitric oxide output using single-breath humming exhalations. European Respiratory Journal, 22, 323 – 329. https://doi.org/10.1183/09031936.03.00017903
Masaoka, Y., & Homma, I. (1997). Anxiety and respiratory patterns: their relationship during mental stress and physical load.. International journal of psychophysiology : official journal of the International Organization of Psychophysiology, 27 2, 153-9. https://doi.org/10.1016/s0167-8760(97)00052-4
Miller, J., Pegelow, D., Jacques, A., & Dempsey, J. (2005). Skeletal muscle pump versus respiratory muscle pump: modulation of venous return from the locomotor limb in humans. The Journal of Physiology, 563. https://doi.org/10.1113/jphysiol.2004.076422
Münzberg, H., Berthoud, H., & Neuhuber, W. (2023). Sensory spinal interoceptive pathways and energy balance regulation. Molecular Metabolism, 78. https://doi.org/10.1016/j.molmet.2023.101817
Nakayama, H., Smith, C., Rodman, J., Skatrud, J., & Dempsey, J. (2002). Effect of ventilatory drive on carbon dioxide sensitivity below eupnea during sleep.. American journal of respiratory and critical care medicine, 165 9, 1251-60. https://doi.org/10.1164/rccm.2110041
Negrini, D. (2022). Morphological, Mechanical and Hydrodynamic Aspects of Diaphragmatic Lymphatics. Biology, 11. https://doi.org/10.3390/biology11121803
Noble, D., & Hochman, S. (2019). Hypothesis: Pulmonary Afferent Activity Patterns During Slow, Deep Breathing Contribute to the Neural Induction of Physiological Relaxation. Frontiers in Physiology, 10. https://doi.org/10.3389/fphys.2019.01176
Noble, D., & Hochman, S. (2019). Hypothesis: Pulmonary Afferent Activity Patterns During Slow, Deep Breathing Contribute to the Neural Induction of Physiological Relaxation. Frontiers in Physiology, 10. https://doi.org/10.3389/fphys.2019.01176
Onyper, S., Mocerine, J., Cote, G., & Burkhard, A. (2025). 0156 Longitudinal Examination of the Effects of Cyclic Breathing on Sleep: A Pilot Study. SLEEP. https://doi.org/10.1093/sleep/zsaf090.0156
Pandekar, P., & Thangavelu, P. (2020). Effect of 4-7-8 Breathing Technique on Anxiety and Depression in Moderate Chronic Obstructive Pulmonary Disease Patients. **.
Papp, L., Klein, D., & Gorman, J. (1993). Carbon dioxide hypersensitivity, hyperventilation, and panic disorder.. The American journal of psychiatry, 150 8, 1149-57. https://doi.org/10.1176/ajp.150.8.1149
Pervichko, E., Mitina, O., Stepanova, O., Konyukhovskaya, Y., & Shishkova, I. (2022). THE ROLE OF THE CORONAVIRUS DANGER PERCEPTIONS IN MEDIATING RESPIRATORY FUNCTION DURING COVID-19 PANDEMIC. PERSONALITY IN A CHANGING WORLD: HEALTH, ADAPTATION, DEVELOPMENT. https://doi.org/10.23888/humj2022104313-328
Puybasset, L., Rouby, J., Mourgeon, E., Cluzel, P., Souhil, Z., Law-Koune, J., Stewart, T., Devilliers, C., Lu, Q., & Roche, S. (1995). Factors influencing cardiopulmonary effects of inhaled nitric oxide in acute respiratory failure.. American journal of respiratory and critical care medicine, 152 1, 318-28. https://doi.org/10.1164/ajrccm.152.1.7599840
Quadt, L., Critchley, H., & Garfinkel, S. (2018). The neurobiology of interoception in health and disease. Annals of the New York Academy of Sciences, 1428. https://doi.org/10.1111/nyas.13915
Quigley, K., Kanoski, S., Grill, W., Barrett, L., & Tsakiris, M. (2021). Functions of Interoception: From Energy Regulation to Experience of the Self. Trends in Neurosciences, 44, 29-38. https://doi.org/10.1016/j.tins.2020.09.008
Ramakers, I., Van Den Houte, M., Van Oudenhove, L., Van Den Bergh, O., & Bogaerts, K. (2022). End-Tidal CO_2 in Patients with Panic Disorder, Stress-Related or Functional Syndromes, Versus Healthy Controls. Applied Psychophysiology and Biofeedback, 48, 149-157. https://doi.org/10.1007/s10484-022-09573-z
Ran, C., Boettcher, J., Kaye, J., Gallori, C., & Liberles, S. (2022). A brainstem map for visceral sensations. Nature, 609, 320 – 326. https://doi.org/10.1038/s41586-022-05139-5
Raymann, R., Swaab, D., & Van Someren, E. (2005). Cutaneous warming promotes sleep onset.. American journal of physiology. Regulatory, integrative and comparative physiology, 288 6, R1589-97. https://doi.org/10.1152/ajpregu.00492.2004
Ringer, S., Clausen, N., Spielmann, N., & Weiss, M. (2019). Effects of moderate and severe hypocapnia on intracerebral perfusion and brain tissue oxygenation in piglets. Pediatric Anesthesia, 29, 1114 – 1121. https://doi.org/10.1111/pan.13736
Ringer, S., Clausen, N., Spielmann, N., & Weiss, M. (2020). Effects of hypothermia and hypothermia combined with hypocapnia on cerebral tissue oxygenation in piglets. Pediatric Anesthesia, 30, 970 – 976. https://doi.org/10.1111/pan.13943
Ristiniemi, H., Perski, A., Lyskov, E., & Emtner, M. (2014). Hyperventilation and exhaustion syndrome. Scandinavian Journal of Caring Sciences, 28, 657 – 664. https://doi.org/10.1111/scs.12090
Rossaint, R., Falke, K., López, F., Slama, K., Pison, U., & Zapol, W. (1993). Inhaled nitric oxide for the adult respiratory distress syndrome.. The New England journal of medicine, 328 6, 399-405. https://doi.org/10.1056/nejm199302113280605
Rovira, I. (2021). Nitric oxide. Reactions Weekly, 623, 10. https://doi.org/10.1007/s40278-021-91789-0
Sakurai, M., Hu, A., Yamaguchi, T., Tabuchi, M., Ikarashi, Y., & Kobayashi, H. (2023). Conscious Slower Breathing Predominates Parasympathetic Activity and Provides a Relaxing Effect, in Healthy Japanese Adult Women. Health. https://doi.org/10.4236/health.2023.159064
Salah, H., Goldberg, L., Molinger, J., Felker, G., Applefeld, W., Rassaf, T., Tedford, R., Mirro, M., Cleland, J., & Fudim, M. (2022). Diaphragmatic Function in Cardiovascular Disease: JACC Review Topic of the Week.. Journal of the American College of Cardiology, 80 17, 1647-1659. https://doi.org/10.1016/j.jacc.2022.08.760
Scheibner, H., Bogler, C., Gleich, T., Haynes, J., & Bermpohl, F. (2017). Internal and external attention and the default mode network. NeuroImage, 148, 381-389. https://doi.org/10.1016/j.neuroimage.2017.01.044
Schramm, P., Schneiderman, E., Hui, J., German, Z., Stenberg, W., & Lin, J. (2024). Obstructive sleep apnea mouth breathing phenotype response to combination oral appliance therapy. Frontiers in Sleep, 3. https://doi.org/10.3389/frsle.2024.1272726
Schulz, A., & Vögele, C. (2015). Interoception and stress. Frontiers in Psychology, 6. https://doi.org/10.3389/fpsyg.2015.00993
Sekyonda, Z., An, R., Goreke, U., Man, Y., Monchamp, K., Bode, A., Zhang, Q., El-Gammal, Y., Kityo, C., Kalfa, T., Akkus, O., & Gurkan, U. (2024). Rapid measurement of hemoglobin-oxygen dissociation by leveraging Bohr effect and Soret band bathochromic shift. The Analyst, 149, 2561 – 2572. https://doi.org/10.1039/d3an02071a
Seol, J., Kokudo, C., Park, I., Zhang, S., Yajima, K., Okura, T., & Tokuyama, K. (2023). Energy metabolism and thermoregulation during sleep in young and old females. Scientific Reports, 13. https://doi.org/10.1038/s41598-023-37407-3
Sévoz-Couche, C., & Laborde, S. (2022). Heart rate variability and slow-paced breathing:when coherence meets resonance. Neuroscience & Biobehavioral Reviews, 135. https://doi.org/10.1016/j.neubiorev.2022.104576
Shah, F., & Stål, P. (2022). Myopathy of the upper airway in snoring and obstructive sleep apnea. Laryngoscope Investigative Otolaryngology, 7, 636 – 645. https://doi.org/10.1002/lio2.782
Shao, R., Man, I., & Lee, T. (2024). The Effect of Slow-Paced Breathing on Cardiovascular and Emotion Functions: A Meta-Analysis and Systematic Review. Mindfulness, 1-18. https://doi.org/10.1007/s12671-023-02294-2
Sieck, G., & Fogarty, M. (2025). Diaphragm Muscle: A Pump That Can Not Fail.. Physiological reviews. https://doi.org/10.1152/physrev.00043.2024
Silva, D., De Castro Corrêa, C., & Weber, S. (2024). Orofacial myofunctional and polysomnographic characteristics of children with Down syndrome and obstructive sleep apnea: a pilot study. CoDAS, 36. https://doi.org/10.1590/2317-1782/20242023119en
Siripajana, P., Chalidapongse, P., Sanguanwong, N., & Chaweewannakorn, C. (2024). Efficacy of oropharyngeal exercises as an adjuvant therapy for obstructive sleep apnea: A randomized controlled trial.. Journal of prosthodontic research. https://doi.org/10.2186/jpr.jpr_d_23_00041
Soffer-Dudek, N. (2017). Arousal in Nocturnal Consciousness: How Dream- and Sleep-Experiences May Inform Us of Poor Sleep Quality, Stress, and Psychopathology. Frontiers in Psychology, 8. https://doi.org/10.3389/fpsyg.2017.00733
Stanek, A., Brożyna-Tkaczyk, K., & Myśliński, W. (2021). Oxidative Stress Markers among Obstructive Sleep Apnea Patients. Oxidative Medicine and Cellular Longevity, 2021. https://doi.org/10.1155/2021/9681595
Suess, W., Alexander, A., Smith, D., Sweeney, H., & Marion, R. (1980). The effects of psychological stress on respiration: a preliminary study of anxiety and hyperventilation.. Psychophysiology, 17 6, 535-40. https://doi.org/10.1111/j.1469-8986.1980.tb02293.x
Szymusiak, R. (2016). Thermoregulation During Sleep. **. https://doi.org/10.1016/b978-0-12-809324-5.02772-3
Tolin, D., O’Bryan, E., Davies, C., Diefenbach, G., & Johannesen, J. (2022). Central and peripheral nervous system responses to chronic and paced hyperventilation in anxious and healthy subjects. Biological Psychology, 176. https://doi.org/10.1016/j.biopsycho.2022.108472
Tomasino, B., & Fabbro, F. (2016). Increases in the right dorsolateral prefrontal cortex and decreases the rostral prefrontal cortex activation after-8 weeks of focused attention based mindfulness meditation. Brain and Cognition, 102, 46-54. https://doi.org/10.1016/j.bandc.2015.12.004
Trova, S., Tsuji, Y., Horiuchi, H., & Shimada, S. (2021). Decrease of Functional Connectivity within the Default Mode Network by a Brief Training of Focused Attention on the Breath in Novices. bioRxiv. https://doi.org/10.1101/2021.02.09.430388
Valsecchi, C., Carlesso, E., Battistin, M., Colombo, S., Cattaneo, E., Gori, F., Langer, T., Grasselli, G., & Zanella, A. (2026). In vitro characterization of hemoglobin oxygen dissociation curves and electrolyte shifts in human blood under varying PCO2. Frontiers in Medicine. https://doi.org/10.3389/fmed.2025.1708274
Van Den Heuvel, C., Noone, J., Lushington, K., & Dawson, D. (1998). Changes in sleepiness and body temperature precede nocturnal sleep onset: Evidence from a polysomnographic study in young men. Journal of Sleep Research, 7. https://doi.org/10.1046/j.1365-2869.1998.00112.x
Vaporidi, K., Akoumianaki, E., Telias, I., Goligher, E., Brochard, L., & Georgopoulos, D. (2019). Respiratory Drive in Critically Ill Patients: Pathophysiology and Clinical Implications.. American journal of respiratory and critical care medicine. https://doi.org/10.1164/rccm.201903-0596so
Vaschillo, E., Vaschillo, B., Buckman, J., Nguyen-Louie, T., Heiss, S., Pandina, R., & Bates, M. (2015). The effects of sighing on the cardiovascular system. Biological Psychology, 106, 86-95. https://doi.org/10.1016/j.biopsycho.2015.02.007
Verma, R., J, J., Goyal, M., Banumathy, N., Goswami, U., & Panda, N. (2016). Oropharyngeal exercises in the treatment of obstructive sleep apnoea: our experience. Sleep and Breathing, 20, 1193-1201. https://doi.org/10.1007/s11325-016-1332-1
Vlemincx, E., Abelson, J., Lehrer, P., Davenport, P., Diest, I., & Bergh, O. (2013). Respiratory variability and sighing: A psychophysiological reset model. Biological Psychology, 93, 24-32. https://doi.org/10.1016/j.biopsycho.2012.12.001
Wójcik, M., Jarząbek-Bielecka, G., Merks, P., Luwański, D., Plagens-Rotman, K., Pisarska-Krawczyk, M., Mizgier, M., & Kędzia, W. (2022). Visceral Therapy and Physical Activity for Selected Dysfunctions, with Particular Emphasis on Locomotive Organ Pain in Pregnant Women—Importance of Reducing Oxidative Stress. Antioxidants, 11. https://doi.org/10.3390/antiox11061118
Yang, X., Xie, S., Wen, Y., & Chen, J. (2025). Obstructive Sleep Apnea and Orofacial Myofunctional Profile in Adults: A Cross-Sectional Study. Nature and Science of Sleep, 17, 2185 – 2199. https://doi.org/10.2147/nss.s545762
Ye, D., Chen, C., Song, D., Shen, M., Liu, H., Zhang, S., Zhang, H., Li, J., Yu, W., & Wang, Q. (2018). Oropharyngeal Muscle Exercise Therapy Improves Signs and Symptoms of Post-stroke Moderate Obstructive Sleep Apnea Syndrome. Frontiers in Neurology, 9. https://doi.org/10.3389/fneur.2018.00912
Young, J., Brampton, W., Knighton, J., Finfer, S., Hospital, J., & Way, H. (1994). Inhaled nitric oxide in acute respiratory failure in adults.. British journal of anaesthesia, 73 4, 499-502. https://doi.org/10.1093/bja/73.4.499
Yu, B., Ichinose, F., Bloch, D., & Zapol, W. (2018). Inhaled nitric oxide. British Journal of Pharmacology, 176, 246 – 255. https://doi.org/10.1111/bph.14512
Yu, X., Fumoto, M., Nakatani, Y., Sekiyama, T., Kikuchi, H., Seki, Y., Sato-Suzuki, I., & Arita, H. (2011). Activation of the anterior prefrontal cortex and serotonergic system is associated with improvements in mood and EEG changes induced by Zen meditation practice in novices.. International journal of psychophysiology : official journal of the International Organization of Psychophysiology, 80 2, 103-11. https://doi.org/10.1016/j.ijpsycho.2011.02.004
Zaccaro, A., Piarulli, A., Laurino, M., Garbella, E., Menicucci, D., Neri, B., & Gemignani, A. (2018). How Breath-Control Can Change Your Life: A Systematic Review on Psycho-Physiological Correlates of Slow Breathing. Frontiers in Human Neuroscience, 12. https://doi.org/10.3389/fnhum.2018.00353
Zaliene, L., Mockute, A., & Levickiene, L. (2025). Breathing Interventions Improve Autonomic Function, Respiratory Efficiency and Stress in Dysfunctional Breathing: A Randomised Controlled Trial. Advances in Respiratory Medicine, 93. https://doi.org/10.3390/arm93060056
Zhao, G., Zhao, Y., Yu, X., Kiprotich, F., Han, H., Guan, R., Wang, R., & Shen, W. (2018). Nitric Oxide Is Required for Melatonin-Enhanced Tolerance against Salinity Stress in Rapeseed (Brassica napus L.) Seedlings. International Journal of Molecular Sciences, 19. https://doi.org/10.3390/ijms19071912
Zheng, Y., Wang, D., Zhang, Y., & Tang, Y. (2019). Enhancing Attention by Synchronizing Respiration and Fingertip Pressure: A Pilot Study Using Functional Near-Infrared Spectroscopy. Frontiers in Neuroscience, 13. https://doi.org/10.3389/fnins.2019.01209


Schreibe einen Kommentar